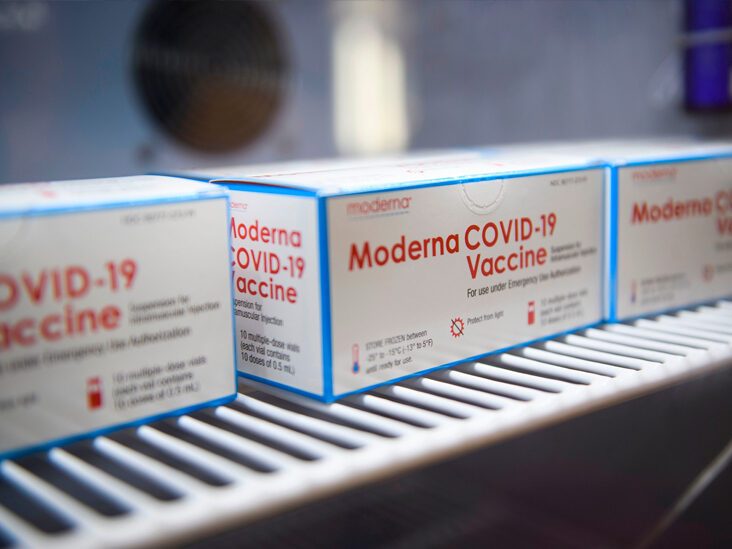
- Die Food and Drug Administration FDA hat das antivirale Remdesivir zugelassen, auch nachdem eine Studie der Weltgesundheitsorganisation WHO einen begrenzten Nutzen gezeigt hat.
- Eine Vorstudie der WHO Solidaritätsprozess von mehr als 11.000 Teilnehmern stellten fest, dass Remdesivir nur einen geringen Einfluss darauf hatte, wie lange Menschen im Krankenhaus blieben, und keinen Einfluss auf den Tod.
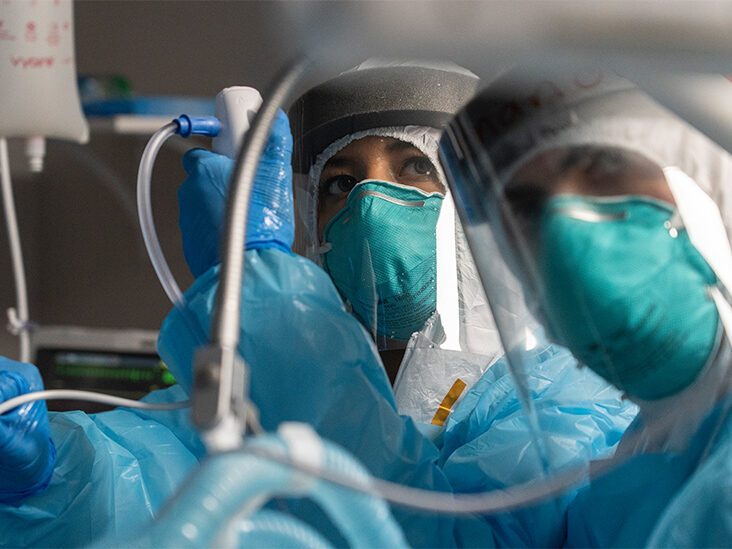
- Ohne einen in den USA zugelassenen COVID-19-Impfstoff sind Ärzte besorgt über eine wirksame Behandlung von COVID-19.
Alle Daten und Statistiken basieren auf öffentlich verfügbaren Daten zum Zeitpunkt der Veröffentlichung. Einige Informationen sind möglicherweise veraltet.
Letzte Woche, die
Dr. Lanny Hsieh , klinischer Professor für Infektionskrankheiten an der UCI Health, sagte, der Schritt der FDA sei „sehr aufregend“.
„Wenn wir alle wissenschaftlichen Erkenntnisse zusammenfassen, die wir bisher über Remdesivir haben, bleibt dies der Standard für die Versorgung von Patienten mit COVID-19 im Krankenhaus“, sagte sie. „Letztendlich würden unsere Patienten von dieser FDA-Zulassung profitieren.”
Die bisherige Forschung zu Remdesivir ist jedoch gemischt, und das Medikament ist weit von einer Heilung für COVID-19 entfernt.
Im Mai gab die FDA eine
Die Agentur
Präsident Trump nahm remdesivir zusammen mit mehrere andere Behandlungen als er Anfang Oktober wegen COVID-19 ins Krankenhaus eingeliefert wurde.
Die FDA stützte ihre Entscheidung auf drei randomisierte kontrollierte Studien.
Eins Studie von 1.062 Teilnehmern mit leichtem, mittelschwerem oder schwerem COVID-19 wurde Anfang Oktober im New England Journal of Medicine veröffentlicht.
Die Ergebnisse dieser Studie zeigen, dass Remdesivir die Dauer des Krankenhausaufenthalts um etwa 5 Tage verkürzte - von 15 auf 10.
Patienten, die Remdesivir einnahmen, hatten auch eine geringere Sterbewahrscheinlichkeit nach 28 Tagen - 11,4 Prozent im Vergleich zu 15,2 Prozent bei Patienten, die ein inaktives Placebo erhielten.
"Diese [Studie] hat zusammen mit anderen von der FDA geprüften Studien zur Zulassung von Remdesivir geführt", sagte Hsieh, der der Hauptprüfer für die klinische Studie von Remdesivir am UCI Medical Center ist.
Die beiden anderen von der FDA überprüften Studien hatten ähnliche Ergebnisse. Eine davon zeigte auch, dass eine 5-tägige Remdesivir-Behandlung genauso gut wirkte wie die Einnahme des Arzneimittels über 10 Tage.
Vorläufige Ergebnisse der Weltgesundheitsorganisation WHO Solidaritätsprozess von mehr als 11.000 Teilnehmern stellten fest, dass Remdesivir nur einen geringen Einfluss darauf hatte, wie lange sie im Krankenhaus blieben, und keinen Einfluss auf den Tod.
Diese Studie wurde als Preprint auf medRxiv veröffentlicht und wurde noch nicht von Experten begutachtet. Daher sollten die Ergebnisse mit einiger Vorsicht betrachtet werden. Die WHO plant dies. veröffentlichen es im New England Journal of Medicine.
Angesichts der Ergebnisse der WHO-Studie stellte Dr. Eric Topol, Professor für Molekulare Medizin am Scripps Research Translational Institute, die Frage, ob die FDA Remdesivir eine vollständige Zulassung hätte erteilen sollen.
"Wie kann Remdesivir eine vollständige [FDA] Zulassung erhalten, wenn es solche gemischten Daten gibt? Diese Entscheidung wird überhaupt nicht unterstützt", schrieb er weiter. Twitter . "Funktioniert es früh? Funktioniert es spät? Funktioniert es jederzeit? So viel ungelöst."
Hsieh sagte jedoch, dass die Studie der WHO mehrere Einschränkungen aufwies, darunter den Vergleich der Remdesivir-Wirkungen mit einem Placebo und die Prüfung mehrerer möglicher Behandlungen in derselben Studie.
„Obwohl interessant, lassen die Ergebnisse von Solidarity die Ergebnisse der [NEJM-Studie] nicht außer Acht“, sagte sie, „eine Studie, die mit der bislang wissenschaftlichsten Genauigkeit durchgeführt wird.“
Ohne einen in den USA zugelassenen COVID-19-Impfstoff sind Ärzte besorgt um eine wirksame Behandlung von COVID-19. Die Zulassung von Remdesivir gibt ihnen endlich etwas, mit dem sie arbeiten können.
"Angesichts des begrenzten Arsenals an wirksamen oder sogar geringfügig wirksamen Behandlungen für COVID-19 und der Tatsache, dass wir keine vollständig kurative Therapie oder keinen Impfstoff haben, ist es gut, mehr Optionen zu haben", sagte Dr. Matthew G. Heinz ein Krankenhausarzt und Internist in Tucson, Arizona.
Aber er sagte, Remdesivir sei in einigen Teilen des Landes immer noch schwer zu bekommen, insbesondere in ländlichen Gebieten.
Und es ist teuer. Eine 5-tägige Behandlung kann kosten 3.120 USD für Personen mit privater Versicherung, berichtet Vox.
Remdesivir ist auch nicht ohne Risiken. Bei manchen Menschen kann es verursachen
„In bestimmten Situationen für bestimmte Patienten halte ich die Anwendung von [Remdesivir] für sinnvoll“, sagte Heinz, „weil es die Virusreplikation hemmen kann - wenn es zum richtigen Zeitpunkt verabreicht wird.“
Remdesivir blockiert die Replikation des Coronavirus, sodass es am besten funktioniert, wenn es frühzeitig verabreicht wird.
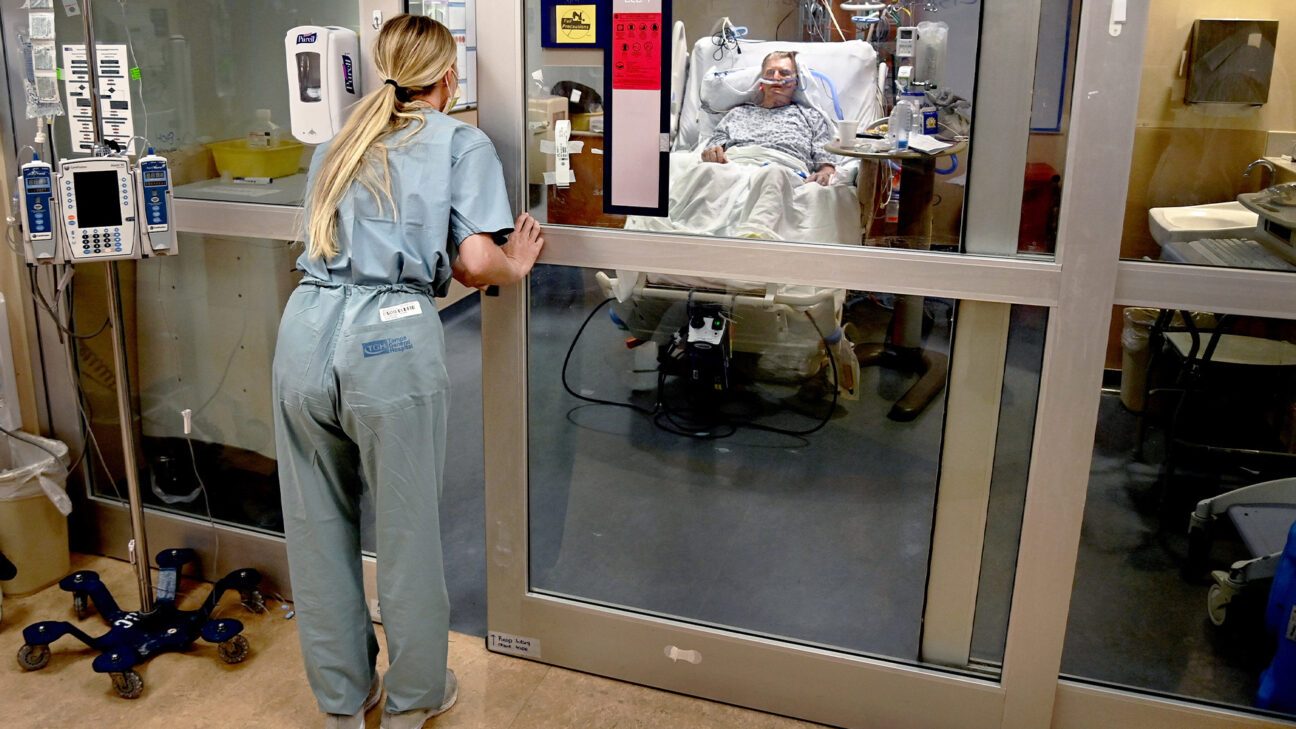
"Remdesivir wird wahrscheinlich nützlicher sein, um das ernsthafte Fortschreiten der Krankheit zu stoppen", sagte Heinz. "Aber es jemandem zu geben, der bereits kritisch ist - intubiert zu werden oder der bereits intubiert wurde - funktioniert möglicherweise nicht."
Das Medikament ist in späteren Stadien von schwerem COVID-19 weniger wirksam, wenn der Schaden eher durch eine überaktive Immunantwort als durch das Virus selbst verursacht wird.
An diesem Punkt wenden sich Ärzte anderen Behandlungen zu, die auf das Immunsystem abzielen. Eine davon ist das Kortikosteroid. Dexamethason das die Immunantwort dämpft und nachweislich die Todesfälle durch COVID-19 reduziert.
Obwohl Remdesivir gegen COVID-19 nicht vollständig wirksam ist, sind viele Ärzte an vorderster Front froh, es als Option zu haben.
„Angesichts der Tatsache, dass keine signifikanten Sicherheitsbedenken bestehen und mindestens eine gute Studie einen gewissen Nutzen zeigt, ist es sinnvoll, Remdesivir als verfügbare Behandlung zu haben - während wir auf bessere warten“, sagte Heinz.