Studie besagt, dass ein Drittel der Medikamente nach ihrer Zulassung Sicherheitsprobleme entwickelt. Einige Experten sagen, dass unser Arzneimittelzulassungsverfahren tatsächlich funktioniert.
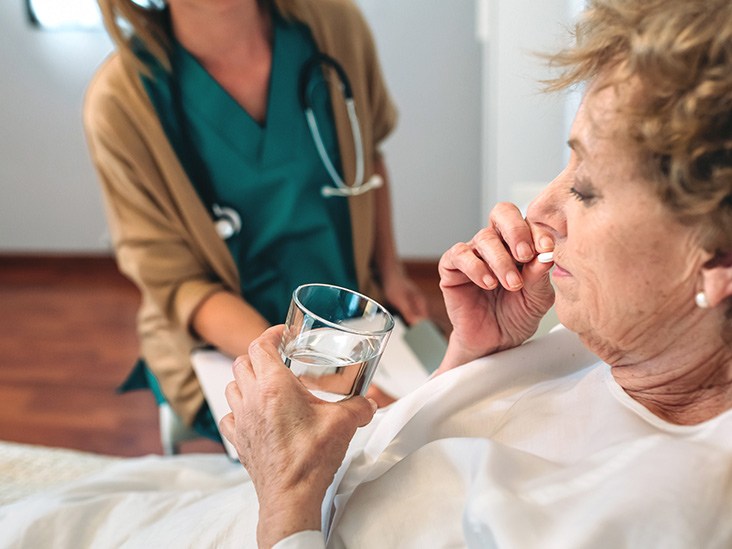
Sobald ein Medikament die Verkaufsregale erreicht, ist es sicher… richtig?
Vielleicht nicht.
In einem neuen
Die Ergebnisse der von Yale geleiteten Studie wurden letzte Woche im Journal der American Medical Association JAMA veröffentlicht.
Während Medikamente jahrelang vor der Zulassung streng getestet werden, konzentrieren sich diese Studien in der Regel auf eine kleine Anzahl von Patienten.
Sobald die Medikamente einer größeren Anzahl von Menschen zur Verfügung gestellt werden, werden immer wieder Probleme auftauchen, sagten die Forscher.
Die Ergebnisse mögen alarmierend klingen, aber von GesundLinie befragte Forscher und Experten sagen, dass dies bedeutet, dass die FDA ihre Arbeit erledigt, indem sie Medikamente nach ihrer Zulassung weiterhin überwacht.
Lesen Sie mehr: Müssen wir den Prozess der Arzneimittelzulassung beschleunigen? »
Das Zulassungsverfahren für Arzneimittel hat viele Facetten.
"Das Zulassungsverfahren der FDA beinhaltet ein Gleichgewicht zwischen klinischem Nutzen und unnötigen oder unerwünschten Ergebnissen in Form von unerwünschten Ereignissen", sagte Jeff Patrick, PharmD, Direktor des Drug Development Institute am Comprehensive Cancer Center der Ohio State University, gegenüber GesundLinie.
"Sicherheit ist für die FDA äußerst wichtig", fügte er hinzu. "Sie müssen den klinischen Nutzen des Patienten, der eine Therapie benötigt, gegen das Risiko abwägen, das ein bestimmtes Medikament darstellen könnte, und wirklich versuchen, dieses Gleichgewicht zu steuern."
Dennoch kann keine bestimmte Anzahl klinischer Studien vorhersagen, wie ein Medikament von der Allgemeinbevölkerung aufgenommen wird.
„Die Zulassung durch die FDA bedeutet nicht, dass wir alles über ein Medikament wissen“, sagte Dr. Nicholas Downing, Erstautor des Forschungspapiers und niedergelassener Arzt für Innere Medizin am Brigham and Women's Hospital in Boston, gegenüber GesundLinie.
„Wenn ein Medikament zugelassen ist, gibt es viele, die wir nicht kennen“, erklärte er. „Wir wissen nicht, ob das Medikament so sicher oder vielleicht nicht so sicher sein wird, wie die FDA es erwartet hatWir wissen nicht, ob das Medikament auf der Grundlage klinischer Beweise vor dem Markteintritt so wirksam sein wird, wie die FDA angenommen hat. Es besteht also von Natur aus eine gewisse Unsicherheit zum Zeitpunkt der MarkteinführungZulassung. Und da Medikamente über einen längeren Zeitraum und in breiteren Bevölkerungsgruppen verwendet werden, lernen wir manchmal neue Informationen. “
Patrick weist darauf hin, dass es bei der Behandlung von Patienten mit Medikamenten niemals einen einheitlichen Ansatz geben kann, da unterschiedliche Menschen unterschiedlich reagieren können.
„Sie wissen nicht, was mit einem bestimmten Patienten passieren kann, bis Sie den Patienten dieser besonderen Situation aussetzen“, sagte er. „Unser Mantra hier im OSU Comprehensive Cancer Center lautet:„ Es gibt keinen Routinekrebs “, und wir meinenDas. Weil jeder Patient auf Therapien unterschiedlich ansprechen kann, abhängig von seinem genetischen Profil oder der Schwere der Krankheit oder so vielen anderen Faktoren. “
Die Tatsache, dass 32 Prozent der Medikamente nach der Zulassung gekennzeichnet sind, bedeutet, dass die FDA ihre Arbeit tut, sagten Experten.
„Die Tatsache, dass für 1 von 3 Medikamenten ein Sicherheitsereignis nach dem Inverkehrbringen festgestellt wurde, zeigt mir, dass die FDA nach diesen Problemen sucht, und das ist wichtig“, sagt Downing. „Es sagt mir, dass die FDA sich nicht fühltdass seine Verantwortung zum Zeitpunkt der Zulassung des Arzneimittels endet. Es sagt mir, dass die FDA ihre Verantwortung für die Gewährleistung der Sicherheit von Arzneimitteln während ihres gesamten Lebenszyklus sehr ernst nimmt. “
"Wenn es keine oder nur sehr wenige Ereignisse gab, muss man sich die Frage stellen, ob die FDA überhaupt nach diesen Dingen sucht", fügte er hinzu.
Patrick stimmt zu.
"Wenn sie diese Medikamente nach der Zulassung nicht überwachen würden, würde es möglicherweise zu einer entspannten Plattform kommen, auf der die Sicherheit möglicherweise nicht so ernst genommen wird", sagte er.
Downing weist darauf hin, dass eine kontinuierliche Überwachung und Prüfung neue Erkenntnisse über Arzneimittel liefern kann, die seit Jahrzehnten auf dem Markt sind.
„Wir führen heute noch klinische Studien mit Aspirin durch“, bemerkte er. „Das ist eines der älteren Medikamente, die wir haben, aber wir finden immer noch neue Wege, das Medikament zu verwenden, und wir lernen immer noch darüber. ”
Lesen Sie mehr: Was ist los mit unseren verschreibungspflichtigen Medikamentenstudien? »
Die neue Forschung basiert auf früheren Arbeiten desselben Teams.
Downing sagt, es gibt noch Erkenntnisse, die sie gerne herausarbeiten möchten.
„Im Durchschnitt ereigneten sich diese Sicherheitsereignisse nach dem Inverkehrbringen 4,2 Jahre nach der Zulassung“, sagte er. „Eine Frage, die Sie möglicherweise stellen: Gibt es eine Möglichkeit, Arzneimittel zu identifizieren, bei denen Sicherheitsprobleme früher auftreten können?Menschen oder die Zeit, die Menschen ein neues Medikament einnehmen, bevor ein neues Sicherheitsereignis ans Licht kommt “, sagte er.„ Ich frage mich, ob es Möglichkeiten und Methoden gibt, mit denen wir die Sicherheit von Medikamenten untersuchen können, mit denen wir sie identifizieren könnenSicherheitsereignisse nach dem Inverkehrbringen schnell oder in kürzerer Zeit als 4,2 Jahre. “
Während bei 32 Prozent der Medikamente Sicherheitsereignisse nach dem Inverkehrbringen festgestellt wurden, fragen sich sowohl Downing als auch Patrick, ob dies die richtige Zahl ist.
"Ehrlich gesagt bin ich überrascht, dass es nur ein Drittel ist", sagte Patrick. "Ich würde es als relativ niedrige Zahl betrachten."
Downing gibt dies wieder.
„Ist 1 zu 3 die richtige Zahl? Ist sie zu hoch, zu niedrig oder genau richtig?“, Fragte er. „Ich weiß es nicht, aber es sagt mir, dass wir nach diesen Dingen suchen undWir finden sie. Diese Sicherheitsereignisse nach dem Inverkehrbringen finden statt und spiegeln die Tatsache wider, dass es Dinge gibt, die wir über neue Medikamente nicht wissen, wenn sie zugelassen sind, und wir erfahren davon, wenn sie in größeren Populationen angewendet werdenfür längere Zeiträume. ”