Beamte der Bundesbehörde sagen, der Hersteller des EpiPen habe die Behauptungen, sein Produkt habe in einigen Fällen nicht richtig funktioniert, nicht untersucht.
FDA-WARNUNG ÜBER EPIPEN-STÖRUNGENIm März 2020 veröffentlichte die Food and Drug Administration FDA a
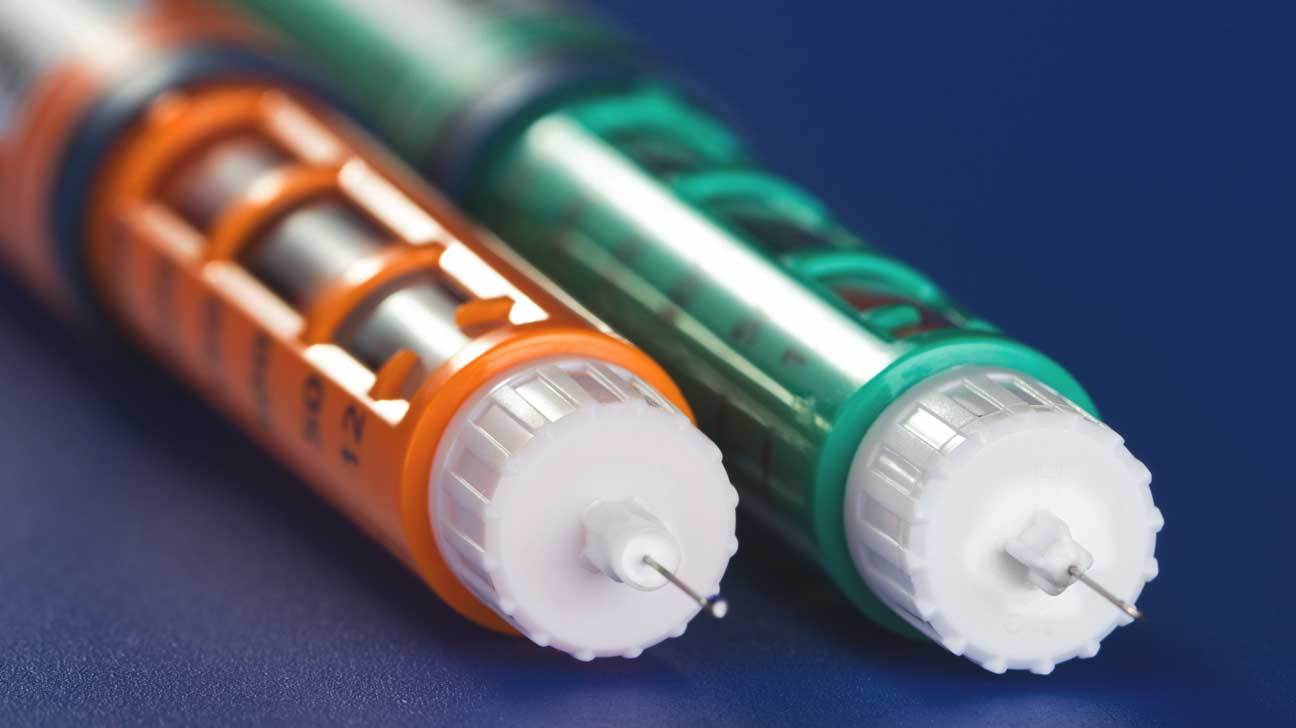
Sicherheitsalarm um die Öffentlichkeit zu warnen, dass Adrenalin-Autoinjektoren EpiPen, EpiPen Jr und generische Formen möglicherweise nicht richtig funktionieren. Dies kann dazu führen, dass Sie im Notfall möglicherweise keine lebensrettende Behandlung erhalten. Wenn Ihnen ein Adrenalin-Autoinjektor verschrieben wird, lesen Sie die Empfehlungenvom Herstellerhier und sprechen Sie mit Ihrem Arzt über die sichere Verwendung.
Sie können Allergikern möglicherweise nicht die Schuld geben, wenn sie heutzutage etwas nervös sind.
„Zu erfahren, dass [der EpiPen] im Notfall wahrscheinlich nicht das Leben meines Kindes retten würde, war alarmierend und ärgerlich“, sagte Lindsay Stril, eine Mutter eines 7-jährigen Mädchens mit schweren Nussallergien im US-Bundesstaat WashingtonGesundLinie.
Stril trug fast ein Jahr lang einen zurückgerufenen EpiPen mit sich herum, den sie im Notfall nie benutzen musste.
„Arzneimittelhersteller von Rettungsmedikamenten müssen strengere Qualitätskontrollen und -tests durchführen, damit durch einen defekten EpiPen niemals Leben verloren gehen“, sagte Stril. „Berichte über defekte Stifte sollten ihre Priorität Nr. 1 sein. Ich denke, sie lassen unsNieder."
Strils Wut tauchte nach einem auf
In einem Brief vom 5. September sagten FDA-Beamte, der Hersteller von EpiPen-Adrenalin-Injektoren habe Herstellungsprobleme, die dazu führten, dass die Geräte nicht richtig funktionierten, nicht ordnungsgemäß untersucht.
FDA-Beamte sagten, dass die Fehler möglicherweise das Leben von Menschen bedrohen, bei denen schwere allergische Reaktionen auftreten.
In ihrem Warnschreiben an Meridian Medical Technologies, eine Abteilung von Pfizer, sagten Beamte, die Agentur habe "Hunderte von Beschwerden erhalten, dass Ihre EpiPen-Produkte in lebensbedrohlichen Notfällen nicht funktionieren, einschließlich einiger Situationen, in denen Patienten später starben."
„Sie [Meridian] haben diese Beschwerden nicht gründlich untersucht“, heißt es in dem FDA-Schreiben. „Darüber hinaus stellen wir fest, dass in Ihrem Follow-up potenziell fehlerhafte Produkte nicht vom Markt genommen wurden, obwohl Sie in einem einen Fehler festgestellt hattender kritischen Komponenten, die zur Herstellung dieser Produkte verwendet wurden, und obwohl Sie letztendlich den gleichen oder einen ähnlichen Komponentenfehler als Hauptursache für mehrere Beschwerden bestätigt haben. “
Die FDA hat Meridian angewiesen, die im Warnschreiben angesprochenen Probleme unverzüglich zu lösen oder mögliche rechtliche Schritte einzuleiten, bis die Produkte des Unternehmens beschlagnahmt und Verfügungen gegen deren Verkauf getroffen wurden.
In einigen Fällen gaben FDA-Beamte an, dass EpiPen- und EpiPen Jr-Produkte letztere für Kinder entwickelt Patienten, die sich einer Anaphylaxie unterzogen, bei Durchführung der richtigen Aktivierungssequenz kein Adrenalin verabreichten.
In anderen Fällen haben die Geräte das Medikament fälschlicherweise abgegeben, wenn es nicht aktiviert wurde, und die Injektoren bei Bedarf leer gelassen.
Die FDA sagte in ihrem Brief an Meridian: „Sie haben mehrere schwerwiegende Komponenten- und Produktfehler für Ihre EpiPen-Produkte, einschließlich Fehler im Zusammenhang mit Todesfällen von Patienten und schwerer Krankheit, nicht gründlich untersucht. Sie haben auch den Umfang Ihrer Untersuchungen zu diesen nicht erweitertschwerwiegende und lebensbedrohliche Fehler oder geeignete Korrekturmaßnahmen bis zur Inspektion durch die FDA. “
Meridian kündigte am 31. März 2017 nach einer FDA-Untersuchung den freiwilligen Rückruf von 13 Chargen potenziell defekter EpiPen-Produkte an.
Meridian stellt EpiPens in einer Fabrik in Brentwood, Missouri, für den Vertreiber von Medizinprodukten Mylan Specialty her.
In einem 8. September Presseerklärung Laut Vertretern von Myland ist das Unternehmen „von der Sicherheit und Wirksamkeit der am Standort hergestellten EpiPen-Produkte überzeugt.“
„Für Technologien, die es schon seit Jahrzehnten gibt, bin ich frustriert, dass wir als Gemeinschaft sogar die Sicherheit unserer Medikamente in Frage stellen müssen“, Allie Bahn, die Blogs als Miss Allergic Reactor über Lebensstil und Reisen für Menschen mit Lebensmittelallergien, sagte GesundLinie.
„EpiPens sind mein Sicherheitsnetz. Wenn ein Fehler auftritt, verlasse ich mich darauf, dass sie mein Leben retten. Stimmt das noch? Ich hoffe es, aber ich habe nicht das gleiche Vertrauen wie früher. Unzuverlässige Medikamente sind es nichtetwas, das jeder von uns berücksichtigen sollte. ”
Der EpiPen-Rückruf war das zweite Mal in zwei Jahren, dass Hersteller fehlerhafte Adrenalininjektoren aus den Apothekenregalen ziehen mussten.
Im Oktober 2015 freiwillig Sanofi US zurückgerufen alle Auvi-Q-Adrenalin-Injektoren vom Markt aufgrund ihres Potenzials für eine ungenaue Dosierungsabgabe, einschließlich „Nichtabgabe des Arzneimittels“.
Der Auvi-Q-Rückruf basierte auf 26 Kundenbeschwerden im Vergleich zu den Hunderten, die Meridian über EpiPen erhalten hatte.
Auvi-Q war wieder eingeführt auf den Markt im Oktober 2016, nachdem sie von ihren Erfindern über das in Privatbesitz befindliche Pharmaunternehmen kaléo Pharma von Sanofi zurückgekauft wurden.
Das Unternehmen „führte eine gründliche Bewertung der Herstellung durch und investierte in neue Technologien und Qualitätssysteme, um eine genaue, zuverlässige und konsistente Lieferung des Produkts sicherzustellen“, heißt es in einer Pressemitteilung.
Bahn, eine lebenslange Benutzerin von EpiPens, erhielt ein Rezept für Auvi-Q, als es erstmals veröffentlicht wurde, weil sie als Läuferin das kompakte Design schätzte.
„Als Auvi-Q vom Markt ging, hatte ich das Glück, dass ich immer noch EpiPens bei mir hatte. Jetzt bin ich mir nicht sicher, was ich denken soll“, sagte sie. „Als Auvi-Q zurückkam, war ich versucht, ein Rezept zu bekommenAber im Hinterkopf fühlte ich mich angesichts der Vergangenheit immer noch unwohl, mich darauf zu verlassen. Seit den Nachrichten mit EpiPen rief ich meinen Allergologen an, um ein Rezept für Auvi-Q anzufordern. “
"Im Moment", fügte sie hinzu, "habe ich kein großes Vertrauen in beide und bin frustriert, dass dies die einzigen Optionen sind."